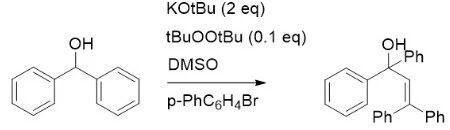
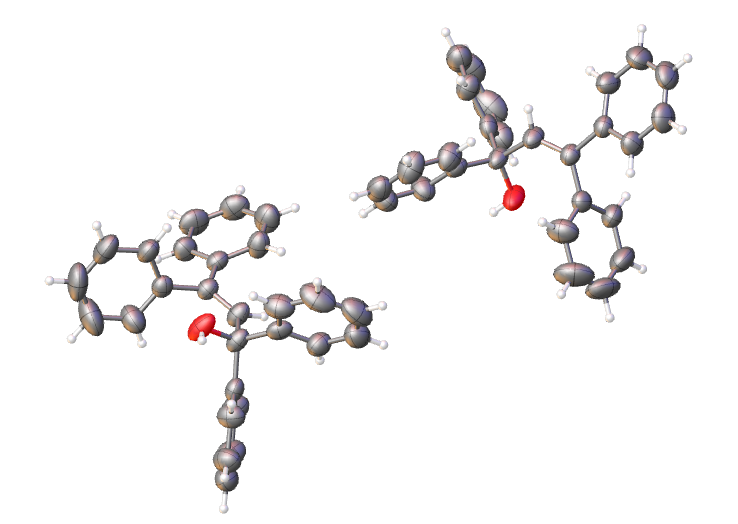
最近在探索一个设计出来的反应的过程中,意外得到了一个乍看起来令人惊讶的产物。
在最早的探索中,在氮气保护下,将0.1 mmol 二苯甲醇、2 eq KOt-Bu溶于3 mL DMSO中,加入0.1 eq t-BuOOt-Bu,60 ℃加热半小时,溶液变为深绿色。加入0.1 mmol 3,5-二甲氧基溴苯在1 mL DMSO中的溶液,体系迅速变为金黄色。继续加热1 h,芳基溴完全消失,出现1个主要产物。用盐水淬灭、乙酸乙酯萃取,柱色谱分离(PE:EA=10:1),得到4.1 mg无色油状物。经NMR、GC-MS鉴定,推测结构为2-甲硫基取代的苯酚。由于产物没有标准谱图,也有可能是甲硫基与羟基交换位置的异构体。
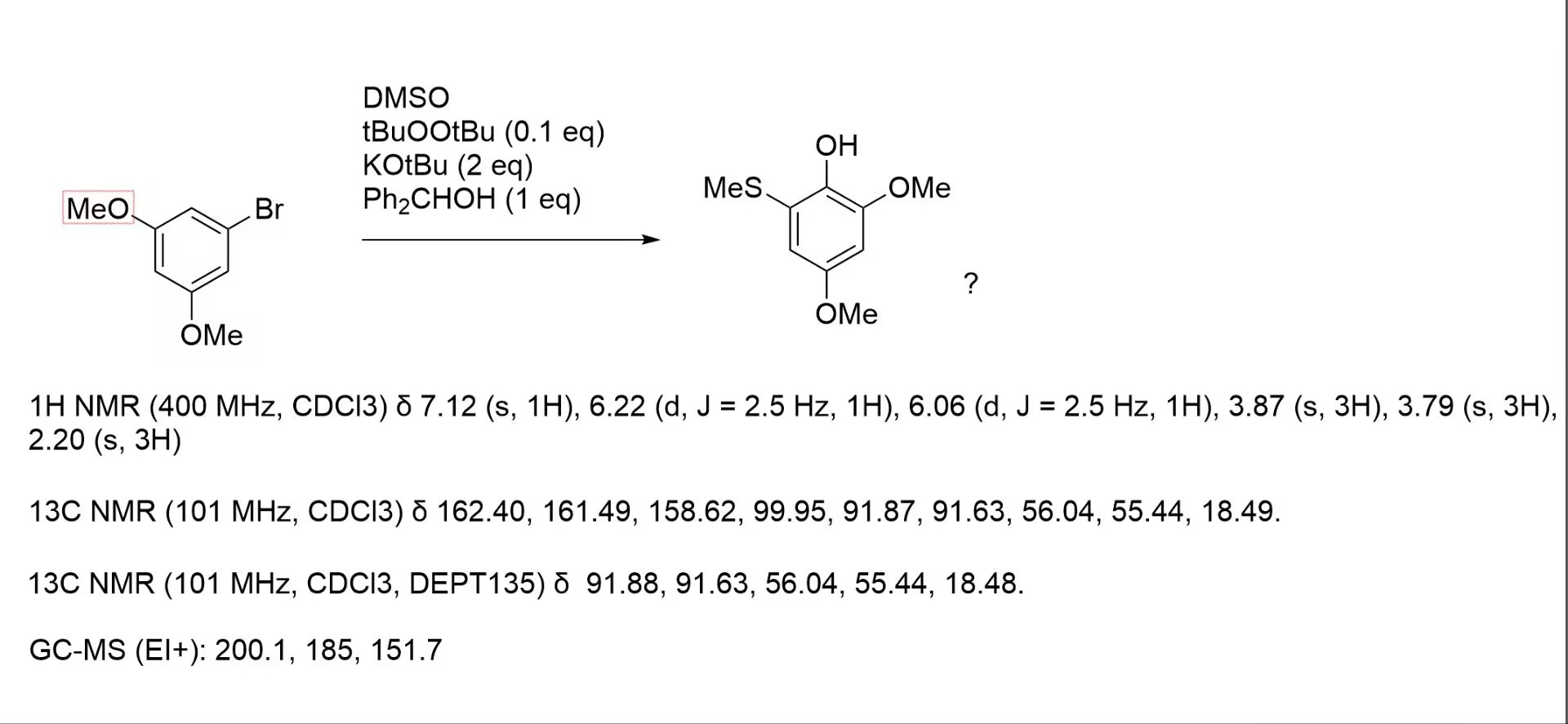
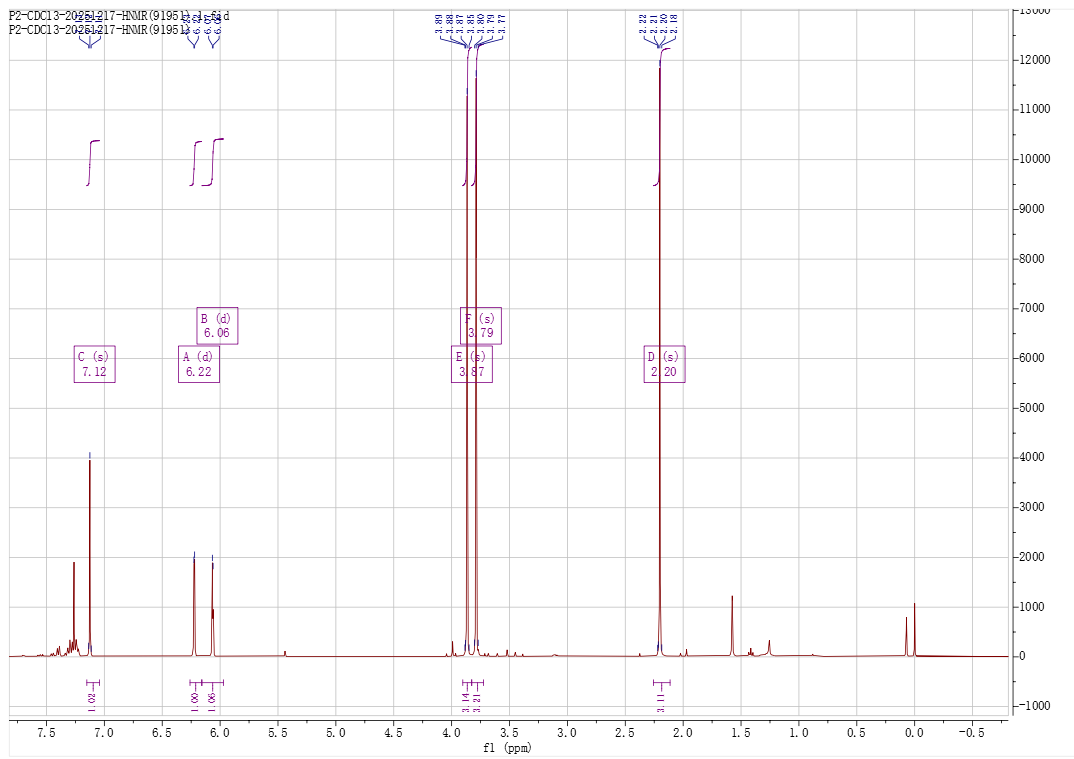
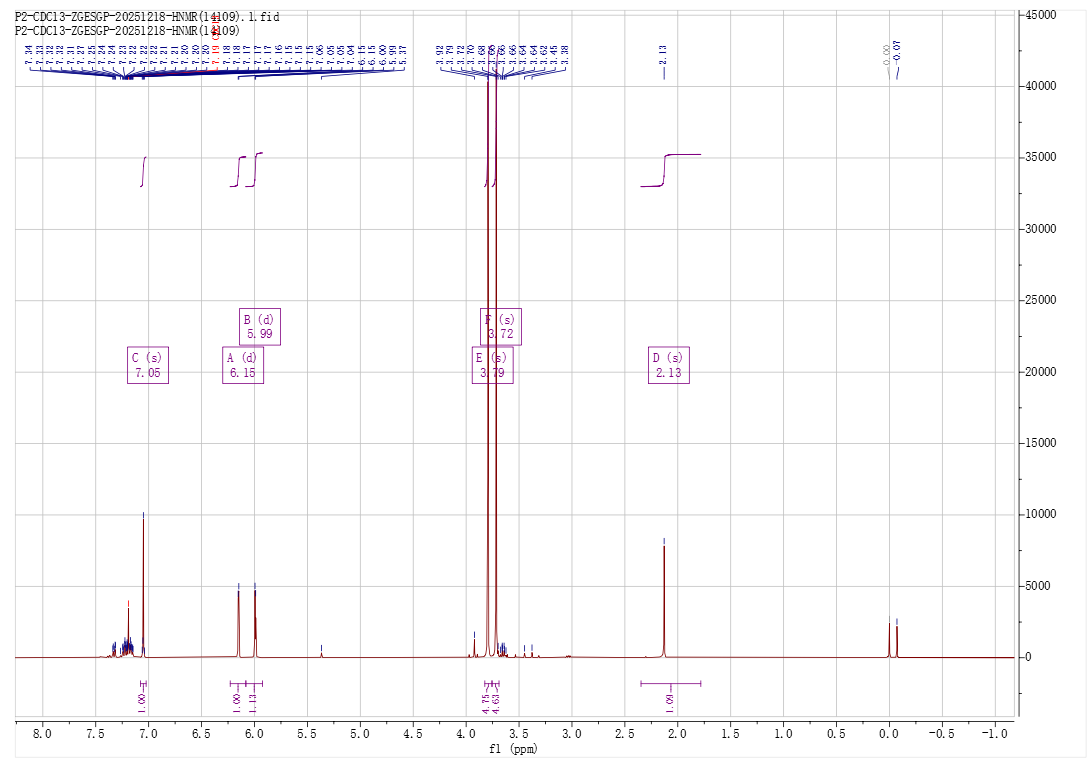
图1. 反应式和产物的1H-NMR谱图(氘代氯仿)
6.06 ppm和6.22 ppm的两个氢原子(J=2.5 Hz)提示存在且仅存在两个间位氢原子的四取代苯环,因此7.12 ppm的单峰应该是酚羟基或巯基氢。推测这是羟基氢,而2 ppm左右的3H(s)是甲硫基氢。
然而,氘代氯仿中的重水交换实验的结果令人十分困惑:所有峰都仍然存在且保持尖锐,低场处3个峰比例保持1:1:1,如果以这三个峰为1H,则甲氧基 变成了4H,2.13 ppm处则变成了1H!
在DMSO中的核磁则清晰得多。该化合物在DMSO中给出如下 氢谱信号:1H NMR (400 MHz, DMSO) δ 9.36 (s, 1H), 6.11 (d, J = 2.5 Hz, 1H), 6.08 (d, J = 2.5 Hz, 1H), 3.76 (s, 3H), 3.70 (s, 3H), 2.12 (s, 3H).重水交换后,9.36 ppm处单峰消失,且其他峰保持不变,从而验证了活泼氢的存在。
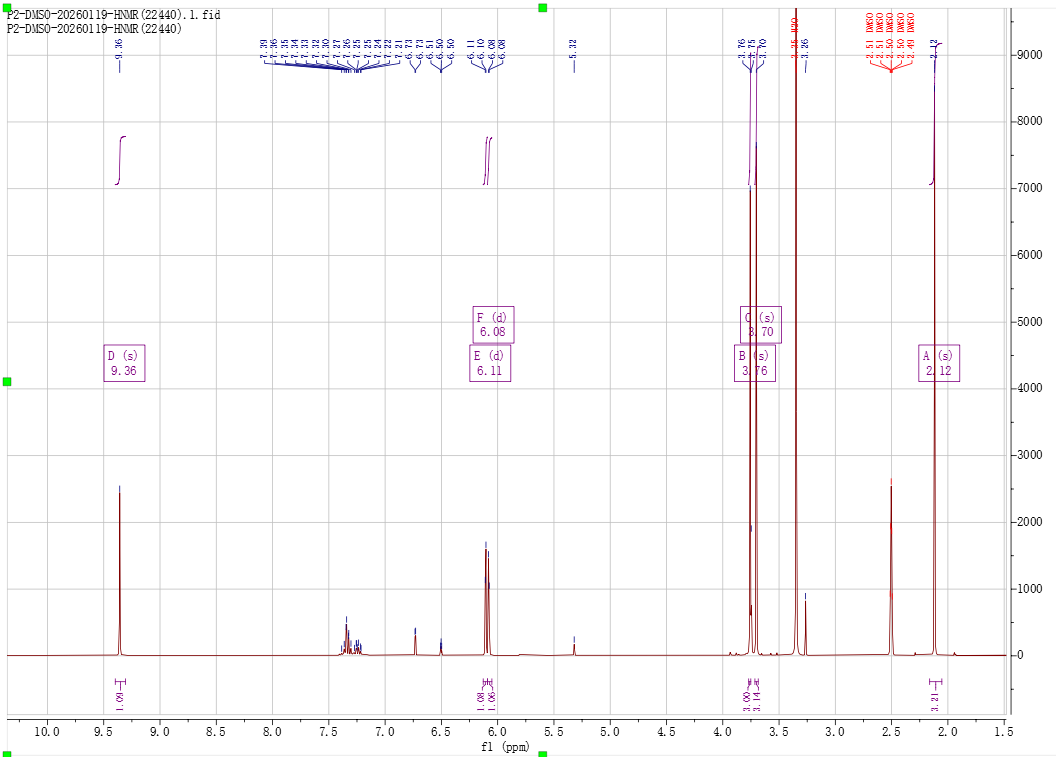
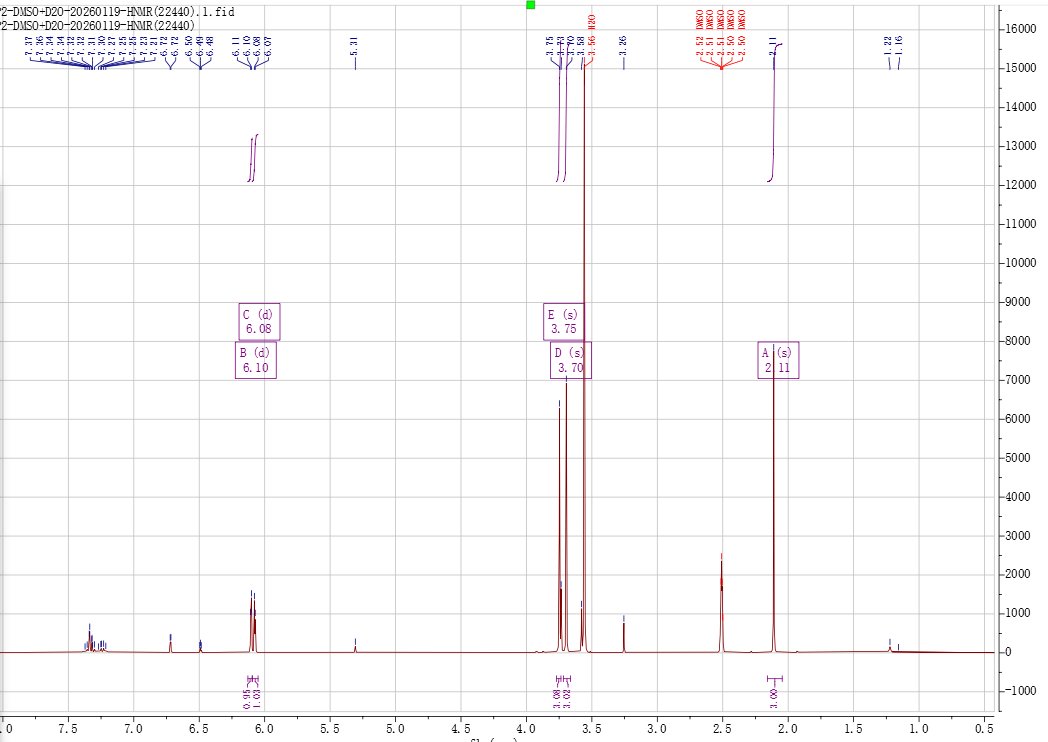
图2. 产物的1H-NMR谱图(氘代DMSO)
显然,产物必须由DMSO参与生成。保持其他条件相同,更换溶剂为DMF、MeCN、THF,均无法得到该产物,仅有芳基溴大量回收。KOt-Bu促进的该反应产率不高,且可重复性不佳;事实上,在上述条件下我只成功得到了2次该产物,且使用新开的超干DMSO并不能确保反应成功。对碱的筛选表明,DBN、Cs2CO3、NaH都完全无法带来产物,但NaHMDS能有效促进该反应,产率定量,且可重复性很高。
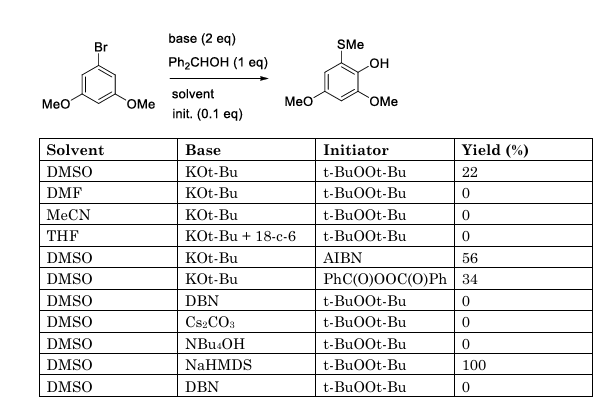
表1. 多种条件下的产率
为了确定反应机理,进行了2个对比实验。用过氧化苯甲酰与DMSO、碱共热,未生成任何可检测到的2-甲硫基酚产物,说明芳基自由基不是反应的关键中间体。而将芳基溴、NaHMDS在DMSO中共热, 不需要二苯甲醇和自由基引发剂,就可以定量生成产物。因此,这一反应实际上仅需要强碱和DMSO的存在!
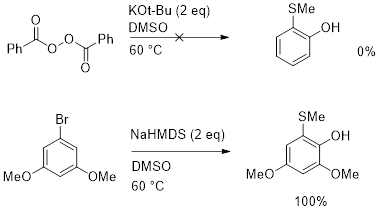
图3. 对照实验
根据上述事实,可以猜测反应经历苯炔中间体。事实上,这类反应并非是第一次发现,在文献中早就有迹可循。2014年,肖文精报道了一系列此类反应(10.1021/ol501638x),使用2-氟代三甲基苯基硅烷作为苯炔前体,与DMSO反应并裂解S--O键,随后用亲电试剂捕获产生的酚阴离子,得到了2-甲硫基-1-烷氧基芳烃。这类反应后续又被发现多种变体,如2017年的苯炔裂解二芳基亚砜生成硫鎓盐的反应(10.1021/acs.orglett.6b03840)。因此,这个意外发现实则并非新反应,而是强碱性条件下的苯炔转化的另一个例子 。

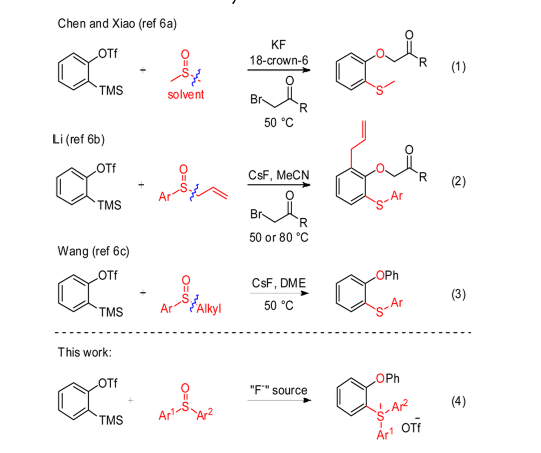
图4. 相关文献报道
附录. 另一个更诡异的反应
3,5-二甲氧基溴苯在该条件下的转化可认为是经由苯炔中间体。但如果以4-苯基溴苯为底物,则会生成一个完全不同的二苯甲醇自缩合产物。在1 mmol scale下,产率为56%。它又是怎么生成的呢?